Kimia SMA XI IPA : Termokimia - Sistem dan lingkungan
Kimia SMA XI IPA : Termokimia - Sistem dan lingkungan - Presentation Transcript
- TERMOKIMIASistem dan Lingkungan
OLEH :
Kevin Adrianus
XIA3 / 22 - PENDAHULUAN Sekilas Termokimia
Bagiandariilmukimia yang mempelajariperubahankalorataupanassuatuzat yang menyertaisuatureaksiatauproseskimiadanfisikadisebuttermokimia
Secaraoperasionaltermokimiaberkaitandenganpengukurandanpernafsiranperubahankalor yang menyertaireaksikimia, perubahankeadaan, danpembentukanlarutan. - BAHAN KAJIAN TERMOKIMIA
Bahan kajian termokimia adalah penerapan hukum kekekalan energi dan hukum termodinamika I dalam bidang kimia
Hukum kekekalan energi berbunyi :
Energi tidak dapat diciptakan dan tidak dapat dimusnahkan.
Energi dapat berubah bentuk menjadi energi lain.
Hukum termodinamika I berbunyi :
“Jumlah total energi dalam alam semesta konstan atau tetap” - SISTEM DAN LINGKUNGAN
Dalamtermokimiaadaduahal yang perludiperhatikan yang menyangkutperpindahanenergi, yaitusistemdanlingkungan.
Segalasesuatu yang menjadipusatperhatiandalammempelajariperubahanenergidan berubah selama proses berlangsung disebutsistem.
sedangkanhal-hal yang tidak berubah selama proses berlangsung dan yang membatasisistemdandapatmempengaruhisistemdisebutlingkungan. - SISTEM
Berdasarkan interaksinya dengan lingkungan, sistem dibedakan menjadi tiga macam, yaitu :
Sistem Terbuka
Sistem terbuka adalah suatu sistem yang memungkinkan terjadi perpindahan energi dan zat (materi) antara lingkungan dengan sistem. Pertukaran materi artinya ada hasil reaksi yang dapat meninggalkan sistem (wadah reaksi), misalnya gas, atau ada sesuatu dari lingkungan yang dapat memasuki sistem.- SistemTertutup
- SistemTerisolasi
- PERCOBAAN
Seng dan Asam Klorida - Percobaan antara Seng dan Asam KloridaPercobaan I
Pada percobaan ini, kalor yang dibebaskan sebesar 59 Kj/mol
Sistemnya adalah logam Zn dan larutan HCl
Percobaan ini merupakan sistem terbuka
Lingkungan dalam percobaan ini antara lain : udara sekitar, termometer, pengaduk, dan gelas kimia. - Percobaan antara Seng dan Asam KloridaPercobaan II
Pada percobaan ini, kalor yang dibebaskan sebesar 60,1 kJ/mol
Sistemnya adalah logam Zn dan larutan HCl
Percobaan ini merupakan sistem terutup
Lingkungan dalam percobaan ini antara lain : udara sekitar, termometer, pengaduk, gelas kimia, gelas plastik sebagai insulator - ENTALPI
Entalpi (H) adalah jumlah kalor yang terkandung dalam sistem pada kondisi tekanan tetap.
Entalpi tidak dapat diukur, yang dapat diukur adalah perubahan dari entalpi tersebut (ΔH).
Satuan energi kalor adalah joule (J) dan kalori (kal). Dengan konversi I kal = 4,18 J.
Satu kalori adalah kalor yang diperlukan untuk menaikkan suhu 1 gram sebesar 1°C. - ENTALPI
Berikut adalah hubungan antara entalpi sebelum dan sesudah reaksi :- Entalpi reaktan atau pereaksi dinyatakan dengan HR
- Entalpi produk atau hasil reaksi dinyatakan dengan HP
- Perubahan entalpi dinyatakan dengan ΔH
- REAKSI EKSOTERM
Reaksi eksoterm adalah reaksi kimia yang membebaskan kalor. Kalor berasal dari sebagian entalpi sistem yang dilepas ke lingkungan sehingga entalpi sistem berkurang.
pada reaksi eksosterm, sistem membebaskan energi, sehingga entalpi sistem akan berkurang, artinya entalpi produk lebijh kecil daripada entalpi pereaksi. Oleh karena itu, perubahan entalpinya bertanda negatif. Sehingga :
∆H =HP – HR - Energi Aktivasi
ΔH<0
Dari grafik diatas, dapat dilihat bahwa ∆H =HP – HR. Karena HP lebih kecil daripada HR. Maka ∆H < 0 - Contoh reaksi eksoterm (pembakaran metana) dapat dilihat pada animasi berikut ini :
- REAKSI PEMBAKARAN METANA
Tanda (+) pada 887 kJ disebelah kanan menunjukkan kalor yang dilepas adalah sebesar 887 kJ. Sehingga reaksinya juga dapat ditulis sebagai berikut : - CONTOH REAKSI EKSOTERM
Contoh lain dari reaksi eksoterm dalam kehidupan sehari-hari antara lain :- Ketika kita memegang tempe, tangan akan terasa hangat
- Ketika kita menyalakan api unggun, panasnya akan terasa walaupun tidak bersentuhan
- Membakar minyak tanah menggunakan kompor minyak
- Respirasi. Karena respirasi menghasilkan panas
- REAKSI ENDOTERM
Reaksi endoterm adalah reaksi kimia yang menyerap kalor. Kalor diambil dari lingkungan sehingga entalpi bertambah.
Pada reaksi endoterm sistem menyerap energi. Oleh karena itu, entalpi sistem akan bertambah, artinya entalpi produk (HP) lebih besar daripada entalpi pereaksi (HR).Akibatnya, perubahan entalpi (∆H), yaitu selisih antara entalpi produk dengan entalpi pereaksi bertanda positif. Sehingga :
∆H =HP – HR - Energi Aktivasi
ΔH > 0
Dari grafik diatas, dapat dilihat bahwa ∆H =HP – HR. Karena HR lebih kecil daripada HP. Maka ∆H > 0 - Contoh dari reaksi endoterm adalah reaksi mencairnya es dalam suatu wadah.
Contoh Reaksi kimia dari peristiwa es mencair adalah :
Tanda (+) pada 6,02 kJ disebelah kiri panah menunjukkan bahwa kalor yang diserap sebesar 6,02 kJ. - REAKSI ES MENCAIR
Dengan demikian, reaksi tersebut juga dapat dituliskan sebagai berikut :
Pada reaksi endoderm, kalor (q) diserap sehingga perubahan entalpinya positif (ΔH > 0). Reaksi tersebut dapat digambarkan pada grafik disamping. - CONTOH REAKSI ENDOTERM
Contoh lain dari reaksi endoterm dalam kehidupan sehari-hari antara lain :- Pelarutan gula. Jika gula dilarutkan, dapat dirasakan ada sedikit rasa dingin ketika gelas dipegang
- Tangan yang terasa dingin ketika bersentuhan dengan alkohol
- proses asimilasi
- Proses fotosintesis tumbuhan
- SEKIAN
Terimakasih Atas Perhatiannya
STRUKTUR ATOM
Atom merupakan komponen dasar dalam mempelajari ilmu kimia. Atom merupakan dasar untuk segala sesuatu di alam semesta. Semua benda yang ada di sekitar kita maupun alam semesta (kita menyebutnya sebagai materi) terdiri dari sekumpulan atom. Menurut Dalton atom merupakan materi yang tidak bisa dibagi lagi tetapi masih punya sifat yang sama seperti aslinya. Analogi untuk pernyataan yang dikemukakan oleh Dalton adalah: jika Anda membagi kertas menjadi dua bagian, lalu dari tiap bagian tersebut dibagi dua lagi sehingga diperoleh bagian terkecil yang tidak bisa lagi untuk dibagi tetapi masih berupa kertas.
Apakah ada yang lebih kecil dari sebuah atom?
Apakah ada bagian dari suatu materi yang lebih kecil dari atom? Tentu ada. Hal ini terungkap oleh J.J Thomson yang menemukan suatu partikel yang lebih kecil dari atom yaitu elektron melalui percobaan yang ia lakukan dengan Tabung Crookes (hampa udara). Perkembangan berikutnya ditemukan inti atom oleh Rutherford, partikel proton oleh Goldstein, dan neutron oleh Chadwick. Jadi sebuah atom terdiri dari 3 partikel kecil yaitu proton dan neutron yang merupakan penyusun inti atom, serta elektron yang berpurar mengelilingi inti atom.
Jadi dapat di simpulkan bahwa:
- atom merupakan penyusun utama suatu materi
- atom terdiri dari tiga partikel yaitu elektron, proton, dan neutron
- atom terdiri atas inti atom yang berisi proton dan neutron, dan elektron yang berputar mengelilingi inti atom melalui lintasan-lintasannya (kulit).
Penentuan Persamaan Laju Reaksi
Metode penentuan persamaan laju reaksi
Metode penentuan persamaan laju reaksi dengan laju awal yaitu dengan melibatkan pengukuran laju reaksi pada awal reaksi untuk beberapa konsentrasi awal zat-zat pereaksi.Metode penentuan persamaan laju reaksi dengan metode terisolasi yaitu semua konsentrasi dari pereaksi dibuat berlebih kecuali untuk satu jenis pereaksi. Sebagai contoh pada reaksi berikut:
A + B --> Produk reaksi
v = vA x vB
Metode penentuan persamaan laju reaksi dengan metode laju terintegrasi banyak digunakan untuk reaksi kompleks di mana persamaan laju reaksinya melibatkan zat-zat pereaksi dan produk reaksi. Di dalam metode laju terintegrasi, terdapat beberapa bentuk persamaan laju yang baku untuk setiap orde reaksi. Selanjutnya kita mencoba mencocokkan data hasil percobaan dengan persamaan laju yang baku tersebut.
Metode laju awal dalam penentuan persamaan laju reaksi
pada materi kimia tentang penentuan persamaan laju reaksi kali ini hanya akan membahas metode laju awal yang umum diajarkan ditingkat Sekolah Menengah Atas SMA.Untuk mengetahui lebih lanjut tentang metode laju awal dalam penentuan persamaan laju reaksi, simak contoh reaksi antara nitrogen oksida NO dengan klorin Cl2 berikut:
2NO(g) + Cl2(g) --> 2NOCl(g)
Terhadap reaksi di atas, dilakukan pengukuran untuk 3 set konsentrasi NO dan Cl2 yang berbeda seperti pada tabel berikut:
Tabel hasil eksperimen laju reaksi NO dengan Cl2 (T = 27oC)
Beberapa hal yang harus dipahami terlebih dahulu sebelum menentukan persamaan laju reaksi adalah sebagai berikut:
- Tetapan laju reaksi (k) bergantung pada jenis reaksi dan suhu reaksi. Satuan untuk k tergantung dari orde reaksi keseluruhan dari persamaan laju reaksi
- Orde reaksi adalah bilangan pangkat yang menyatakan besarnya pengaruh konsentrasi zat pereaksi terhadap laju reaksi.
Dari percobaan 1 dan 2, ketika [Cl2] dibuat 2x lipat ([NO] dibuat tetap), laju reaksinya menjadi 2x lipat dari sebelumnya.
Perhatikan juga percobaan 2 dan 3, ketika [NO] dibuat 2x lipat ([Cl2] dibuat tetap), laju reaksi menjadi 4x lipat dari sebelumnya. Artinya laju reaksi berbanding lurus dengan konsentrasi pereaksi dan/ orde reaksi.
Untuk menentukan persamaan laju reaksi, ikuti prosedur berikut:
A + B --> Produk reaksi
1. Buat persamaan reaksinya : v = k [A]x [B]y
2. Tentukan orde masing-masing pereaksi
Untuk menentukan orde pereaksi A yaitu x, lihat 2 percobaan yang nilai [B] tetap
Untuk menentukan orde pereaksi B yaitu y, lihat 2 percobaan yang nilai [A] tetap
3. Masukkan nilai orde yang telah diperoleh ke dalam persamaan reaksi di atas.
Secara matematis, penentuan persamaan laju untuk data di atas adalah sebagai berikut:
1. Persamaan laju reaksi :
V = k [NO]x [Cl2]y
2. Orde reaksi
Orde pereaksi NO, x . . . ? (percobaan 2 dan 3)
Orde pereaksi Cl2, y . . . ? (percobaan 1 dan 2)
3. Berdasarkan nilai orde masing-masing pereaksi di atas, maka diperoleh persamaan laju reaksi :
V = k [NO]x [Cl2]y
V = k [NO]2 [Cl2]1
V = k [NO]2 [Cl2]
Ada
cara sederhana untuk menghitung orde reaksi dalam penentuan persamaan
laju reaksi. Cara sederhana dalam menentukan persamaan laju reaksi
adalah sebagai berikut:V = k [NO]2 [Cl2]1
V = k [NO]2 [Cl2]
Orde pereaksi NO, x . . . ? (percobaan 2 dan 3)
2x = 4 --> x = 2
Orde pereaksi Cl2, y . . . ? (percobaan 1 dan 2)
2y = 2 --> y = 1
Jadi persamaan reaksinya adalah sebagai berikut:
V = k [NO]2 [Cl2]
Tertarik untuk mempelajarinya lebih lanjut? Klik di sini untuk mendownload materi "Penentuan Persamaan Laju Reaksi"
Persamaan Reaksi Kimia antara Larutan Asam dan Basa
October 13, 2011
HA --> H+ + A- (A- merupakan sisa asam/non logam).
Sedangkan basa merukapakan larutan yang menghasilkan ion OH- dan sisa basanya berupa logam (golongan IA, IIA, Al dan Fe).
BOH --> B+ + OH- (B+ merupakan sisa basa/logam).
Secara umum reaksi asam basa adalah sebagai berikut:
HA + BOH --> BA + H - OH (BA merupakan garam)
Untuk mempermudah dalam menyetarakan reaksi asam basa, maka saya membaginya dalam 4 kelompok.
Kelompok 1: Larutan asam yang bervalensi 1 (misalnya HCl, HBr, HNO3) dan basa bervalensi 1 (misalnya NaOH, LiOH, KOH); Larutan asam yang bervalensi 2 (misalnya H2S, H2SO4, H2CO3) dan basa bervalensi 2 {Mg(OH)2, Ca(OH)2, Be(OH)2}.
Jika kedua larutan yang bervalensi sama saling berikatan, maka penyetaraan hanya dilakukan pada jumlah atom H pada ruas kiri dan kanan (khusus untuk asam basa bervalensi lebih dari 1)Contoh 1 (Valensi 1): tuliskan persamaan reaksi antara larutan asam clorida dengan larutan natrium hidroksida yang menghasilkan larutan natrium clorida dan air.
HCl(aq) + NaOH(aq) --> NaCl(aq) + H2O(l)
Contoh 2 (Valensi 2): tuliskan persamaan reaksi antara larutan asam sulfat dengan larutan calsium hidroksida yang menghasilkan larutan calsium sulfat dan air.
H2SO4(aq) + Ca(OH)2(aq) --> CaSO4(aq) + 2 H2O(l)
Kelompok 2: Larutan asam yang bervalensi lebih dari 1 (misalnya H2SO4, H2S, H3PO4) sedangkan basa bervalensi 1 (NaOH, KOH, LiOH).
Aturan yang dipakai dalam menyetarakan reaksi asam basa adalah sebagai berikut:1. Tuliskan persamaan reaksi belum setara
2. Setarakan jumlah sisa basa (logam) pada garam
3. Setarakan jumlah atom H pada kedua ruas
4. Tuliskan persamaan reaksi setara serta wujud zatnya.
Contoh 1: tuliskan persamaan reaksi antara larutan asam sulfat dengan larutan natrium hidroksida yang menghasilkan larutan natrium sulfat dan air.
1. Tuliskan persamaan reaksi belum setara
H2SO4 + NaOH --> Na2SO4 + H2O
2. Setarakan jumlah sisa basa (logam) pada garam: yaitu Na
H2SO4 + 2 NaOH --> Na2SO4 + H2O
3. Setarakan jumlah atom H pada kedua ruas
H2SO4 + 2 NaOH --> Na2SO4 + 2 H2O
4. Tuliskan persamaan reaksi setara serta wujud zatnya.
H2SO4(aq) + 2 NaOH(aq) --> Na2SO4(aq) + 2 H2O(l)
Contoh 2: tuliskan persamaan reaksi antara larutan asam posfat dengan larutan kalium hidroksida yang menghasilkan larutan kalium posfat dan air.
1. Tuliskan persamaan reaksi belum setara
H3PO4 + KOH --> K3PO4 + H2O
2. Setarakan jumlah sisa basa (logam) pada garam: yaitu K
H3PO4 + 3 KOH --> K3PO4 + H2O
3. Setarakan jumlah atom H pada kedua ruas
H3PO4 + 3 KOH --> K3PO4 + 3 H2O
4. Tuliskan persamaan reaksi setara serta wujud zatnya.
H3PO4(aq) + 3 KOH(aq) --> K3PO4(aq) + 3 H2O(l)
Kelompok 3: Larutan asam yang bervalensi 1 (misalnya HCl, HBr, HNO3) sedangkan basa bervalensi lebih dari 1 {Ca(OH)2, Mg(OH)2, Al(OH)3}.
Aturan yang dipakai dalam menyetarakan reaksi asam basa adalah sebagai berikut:1. Tuliskan persamaan reaksi belum setara
2. Setarakan jumlah sisa asam (non logam) pada garam
3. Setarakan jumlah atom H pada kedua ruas
4. Tuliskan persamaan reaksi setara serta wujud zatnya.
Contoh 1: tuliskan persamaan reaksi antara larutan asam clorida dengan larutan magnesium hidroksida yang menghasilkan larutan magnesium clorida dan air.
1. Tuliskan persamaan reaksi belum setara
HCl + Mg(OH)2 --> MgCl2 + H2O
2. Setarakan jumlah sisa asam (non logam) pada garam: yaitu Cl
2 HCl + Mg(OH)2 --> MgCl2 + H2O
3. Setarakan jumlah atom H pada kedua ruas
2 HCl + Mg(OH)2 --> MgCl2 + 2 H2O
4. Tuliskan persamaan reaksi setara serta wujud zatnya.
2 HCl(aq) + Mg(OH)2(aq) --> MgCl2(aq) + 2 H2O(l)
Contoh 2: tuliskan persamaan reaksi antara larutan asam nitrat dengan larutan aluminium hidroksida yang menghasilkan larutan aluminium nitrat dan air.
1. Tuliskan persamaan reaksi belum setara
HNO3 + Al(OH)3 --> Al(NO3)3 + H2O
2. Setarakan jumlah sisa asam pada garam: yaitu NO3
3 HNO3 + Al(OH)3 --> Al(NO3)3 + H2O
3. Setarakan jumlah atom H pada kedua ruas
3 HNO3 + Al(OH)3 --> Al(NO3)3 + 3 H2O
4. Tuliskan persamaan reaksi setara serta wujud zatnya.
3 HNO3(aq) + Al(OH)3(aq) --> Al(NO3)3(aq) + 3H2O(l)
Kelompok 4: Larutan asam bervalensi 2 (misalnya H2S, H2SO4, H2CO3) sedangkan basa bervalensi 3 {Fe(OH)3, Al(OH)3}; atau Larutan asam bervalensi 3 (H3PO4) sedangkan basa bervalensi 2 {Mg(OH)2, Ca(OH)2}
Aturan yang dipakai dalam menyetarakan reaksi asam basa adalah sebagai berikut:1. Tuliskan persamaan reaksi belum setara
2. Setarakan jumlah sisa asam pada garam
3. Setarakan jumlah sisa basa pada garam
4. Setarakan jumlah atom H pada kedua ruas
5. Tuliskan persamaan reaksi setara serta wujud zatnya.
Contoh 1: tuliskan persamaan reaksi antara larutan asam karbonat dengan larutan aluminium hidroksida yang menghasilkan larutan magnesium clorida dan air.
1. Tuliskan persamaan reaksi belum setara
H2CO3 + Al(OH)3 --> Al2(CO3)3 + H2O
2. Setarakan jumlah sisa asam pada garam: yaitu CO3
3 H2CO3 + Al(OH)3 --> Al2(CO3)3 + H2O
3. Setarakan jumlah sisa basa pada garam: yaitu Al
3 H2CO3 + 2 Al(OH)3 --> Al2(CO3)3 + H2O
4. Setarakan jumlah atom H pada kedua ruas
3 H2CO3 + 2 Al(OH)3 --> Al2(CO3)3 + 6 H2O
5. Tuliskan persamaan reaksi setara serta wujud zatnya.
3 H2CO3(aq) + 2 Al(OH)3(aq) --> Al2(CO3)3(aq) + 6 H2O(aq)
Contoh 2: tuliskan persamaan reaksi antara larutan asam posfat dengan larutan magnesium hidroksida yang menghasilkan larutan magnesium posfat dan air.
1. Tuliskan persamaan reaksi belum setara
H3PO4 + Mg(OH)2 --> Mg3(PO4)2 + H2O
2. Setarakan jumlah sisa asam pada garam: yaitu PO4
2 H3PO4 + Mg(OH)2 --> Mg3(PO4)2 + H2O
3. Setarakan jumlah sisa basa pada garam: yaitu Mg
2 H3PO4 + 3 Mg(OH)2 --> Mg3(PO4)2 + H2O
4. Setarakan jumlah atom H pada kedua ruas
2 H3PO4 + 3 Mg(OH)2 --> Mg3(PO4)2 + 6 H2O
5. Tuliskan persamaan reaksi setara serta wujud zatnya.
2 H3PO4(aq) + 3 Mg(OH)2(aq) --> Mg3(PO4)2(aq) + 6 H2O(aq)
Persamaan reaksi pembakaran hidrokarbon, klik di sini.
Tata Nama Senyawa Ion
October 15, 2011
Ion positif disebut juga sebagai kation, dapat berupa kation monoatomik/ion logam (Na+, K+, Li+, Ca2+, Mg2+, Al3+, etc) maupun kation poliatomik seperti NH4+.
Ion negative disebut juga sebagai anion, dapat berupa anion monoatomik/ion non logam (F-, Cl-, Br-, I-, O2-, S2-) maupun anion poliatomik (OH-, NO3-, CO32-, SO42-, PO43-, etc).
Sebelum menuliskan nama senyawa ion, alangkah baiknya mengenal beberapa kation dan anion yang disajikan pada table berikut ini. Untuk kation dan anion yang lebih beragam, dapat di download di sini. (belum tersedia)
Berbagai Jenis Ion
Daftar nama kation/ion positif/ion logam
Daftar nama anion/ion negatif/ion non logam
Penulisan rumus senyawa ion
jika kita sudah mengetahui berbagai jenis ion, langkah selanjutnya adalah menuliskan rumus senyawa ion jika kation dan anion di atas saling berikatan. Penulisan rumus senyawa ion dilakukan dengan ketentuan sebagai berikut:- Kation/ion positif/ion logam ditulis terlebih dahulu
- Senyawa haruslah netral, sehingga jumlah muatan positif dan muatan negative sama dengan cara mengatur indeks kation dan anion.
K+ + Cl- --> KCl (Kalium clorida) | Jumlah muatan positif dan negatif sudah sama.
Ca2+ + 2Cl- --> NaCl2 (natrium klorida) | Jumlah muatan positif 2x muatan negative sehingga ion negative x 2
Mg2+ + SO42- --> MgSO4 (magnesium sulfat) | Jumlah muatan positif dan negative sudah sama
Al3+ + 3Br- --> AlBr3 (aluminium bromide) | Jumlah muatan positif 3x muatan negative sehingga ion negatif x 3
Rumus senyawa ion berkaitan dengan persamaan reaksi kimia yang dapat Anda simak di sini.
Penamaan Senyawa Ion
Jika Anda telah memahami berbagai jenis ion dan penulisan rumus senyawa ion, mudah bagi Anda untuk memberikan tata nama/penamaan senyawa ion. Berikut aturan dalam menuliskan tata nama senyawa ion dengan acuan nama dari berbagai jenis kation dan anion sudah Anda ketahui:1. Nama logam/ion positif/kation disebutkan terlebih dahulu, diikuti nama non logam/ion negative/anion dengan akhiran -ida, seperti pada contoh berikut:
NaCl : Natrium klorida
MgCO3 : magnesium karbonat
Al(OH)3 : aluminium hidroksida
2. Bila logam/ion positif/kation mempunyai lebih dari satu jenis muatan/bilangan oksidasi seperti Fe2+ dan Fe3+, maka jumlah muatan ditulis dalam tanda kurung “( )” dengan huruf romawi, seperti pada contoh berikut:
Fe(OH)2 : besi(II) hidroksida
FePO4 : besi(III) fosfat
PbSO4 : Timbal(II) sulfat
REAKSI KHAS UNTUK BEBERAPA ANION (IDENTIFIKASI ANION DENGAN UJI ENDAPAN)
September 29, 2011
Identifikasi ion bromine - Br-
Ion Br- dengan gas Cl2 menjadikan larutan bewarna kuning. Jika larutan dikocok dengan karbon disulfide, Br2 yang terjadi akan larut dalam karbon disulfide dan warna larutan akan berubah menjadi cokelat.Reaksinya identifikasinya adalah sebagai berikut:
Cl2(g) + 2Br-(aq) --> 2Cl-(aq) [kuning] + Br2(g)
Br2 larut dalam CS2 à warna cokelat
Identifikasi ion chlorine - Cl-
Ion Cl- dengan larutan perak nitrat terjadi endapan putih, yang larut dalam larutan amoniak.Reaksi identifikasinya adalah sebagai berikut:
Ag+(aq) + Cl-(aq) --> AgCl(s) [putih]
AgCl(s) + 2NH3(aq) --> Ag(NH3)2 + Cl-(aq)
Identifikasi ion karbonat - CO32-
Ion CO32- dengan larutan asam klorida menghasilkan gas karbon dioksida. Jika gas ini dialirkan ke dalam air kapur Ca(OH)2, dapat mengeruhkan air kapur.Reaksi identifikasinya adalah sebagai berikut:
2H+(aq) + CO32-(g) --> H2O(l) + CO2(g)
CO2(g) + Ca2+(aq) + 2OH-(aq) --> CaCO3(s) [putih] + H2O(l)
Identifikasi ion yodida - I-
Ion I- dengan gas Cl2 menjadikan larutan bewarna kuning. Jika dikocok dengan karbon disulfide, I2 yang terjadi larut dalam karbon disulfide dan warna larutan akan berubah menjadi ungu.Reaksi identifikasinya adalah sebagai berikut:
Cl2(g) + 2I-(aq) --> 2Cl-(aq) [kuning] + I2(s)
I2 larut dalam CS2 --> warna ungu
Identifikasi ion nitrat - NO3-
Ion NO3- dengan asam sulfat pekat dan larutan besi(II) sulfat pekat akan menghasilkan suatu cincin cokelat.Reaksi identifikasinya adalah sebagai berikut:
NO3-(aq) + 4H+(aq) + 3e- --> NO(g) + 2H2O(l)
3Fe2+(aq) --> 3Fe3+(aq) + e-
----------------------------------------------------------------------------
NO3-(aq) + 4H+(aq) + 3Fe2+(aq) --> NO(g) + 2H2O(l) + 3Fe3+(aq)
NO(g) + Fe2+(aq) --> FeNO2+(aq) [cokelat]
Identifikasi ion pospat - PO43-
Ion PO43- dengan larutan campuran MgCl2, NH4OH, dan NH4Cl (magnesia mixture) menghasilkan endapan putih.Reaksi identifikasinya adalah sebagai berikut:
Mg2+(aq) + NH4OH(aq) + PO43-(aq) --> MgNH4(s) [putih] + OH-(aq)
Identifikasi ion sulfide - S2-
Ion S2- dengan larutan HCl terbentuk gas H2S yang berbau telur busuk. Gas ini jika dikenakan pada kertas saring yang dicelupkan dalam timbale acetate Pb(CH3COO)2 menyebabkan kertas saring berubah menjadi hitam.Reaksi identifikasinya adalah sebagai berikut:
2H+(aq) + S2-(aq) --> H2S(g)
H2S(g) + Pb2+(aq) --> PbS(s) [hitam] + 2H+(aq)
Identifikasi ion sulfite - SO32-
Ion SO32- dengan larutan asam klorida menghasilkan gas SO2. Gas ini dikenakan pada kertas saring yang telah dicelupkan ke dalam larutan kalium bikromat K2Cr2O7 dan asam sulfat. Gas SO2 akan mengubah warna kertas saring ini dari jingga menjadi hijau.Reaksi identifikasinya adalah sebagai berikut:
2H+(aq) + SO32-(aq) --> H2O(l) + SO2(g)
SO2(g) + 2H2O(l) --> SO42-(aq) + 4H+(aq) + 2e- | x 3
Cr2O72-(aq) + 14H+(aq) + 6e- --> 2Cr3+(aq) + 7H2O(l)
-------------------------------------------------------------------------
Cr2O72-(aq) [jingga] + 3SO2(g) + 2H+(aq) --> 2Cr3+(aq) + 3SO42-(aq) + H2O(l)
Identifikasi ion sulfate - SO42-
Ion SO42- dengan larutan barium klorida dan asam klorida menghasilkan endapan putih.Reaksi identifikasinya adalah sebagai berikut:
Ba2+(aq) + SO42-(aq) --> BaSO4(s) [putih]
Reaksi Kimia dalam Larutan Elektrolit
September 27, 2011
Reaksi asam basa (reaksi penetralan).
Reaksi asam basa atau reaksi penetralan adalah reaksi yang terjadi antara asam (H+) dan basa (OH-) menghasilkan H2O yang bersifat netral.
Adapaun contoh reaksi penetralan adalah sebagai berikut:
1. Reaksi: Asam + Basa --> Garam + Air
HNO3 (aq) + KOH (aq) --> KNO3 (aq) + H2O (l)
H2SO4 (aq) + Ca(OH)2 (aq) --> CaSO4 (aq) + H2O (l)
2. Reaksi: Asam + Oksida Basa --> Garam + Air
2HCl (aq) + CaO (s) --> CaCl2 (aq) + H2O (l)
2HNO3 (aq) + Na2O (s) --> Na(NO3)2 (aq) + H2O (l)
3. Reaksi: Asam + Amonia --> Garam
HCl (aq) + NH3 (g) --> NH4Cl (aq)
H2SO4 (aq) +2 NH3 (g) --> (NH4)2SO4 (aq)
Ammonia (NH3)
termasuk basa yang berupa senyawa molekul sehingga dibedakan dari 2
jenis basa lainnya, yakni senyawa ion yang dapat melepas ion OH- dan okisda basa. Terdapat senyawa molekul basa lainnya seperti metilamina (CH3NH2) tetapi reaksinya tidak umum seperti halnya ammonia.
4. Reaksi: Oksida asam + Basa --> Garam + Air
SO3 (g) + 2NaOH (aq) --> Na2SO4 (aq) + H2O (l)
CO2 (g) + Mg(OH)2 (aq) --> MgCO3 (aq) + H2O (l)
Reaksi Pendesakan Logam
Reaksi pendesakan logam adalah
reaksi di mana logam mendesak kation logam lain atau hydrogen dalam
suatu senyawa. Reaksi ini dapat berlangsung apabila logam berada di
sebelah kiri dari logam/H yang didesak dalam deret Volta. Pada reaksi
ini, produk reaksi berupa endapan logam, gas, dan air.
Deret Volta merupakan urutan unsur-unsur yang disusun berdasarkan
data potensial reduksi. berikut beberapa unsur yang dapat dihapal
berdasarkan urutan potensial reduksinya:
Li - K - Ba - Ca - Na - Mg - Al - Mn - Zn - Fe - Ni - Sn - Pb - (H) - Cu - Hg - Ag - Pt - Au
Adapun contoh reaksi pendesakan logam adalah sebagai berikut:
1. Reaksi: Logam 1 + Garam 1 --> Garam 2 + Logam 2
Zn (s) + CuSO4 (aq) --> ZnSO4 (aq) + Cu (s)
2Al (s) + 3FeSO4 (aq) --> Al2(SO4)3 (aq) + 3Fe (s)
Cu (s) + Na2SO4 (aq) --> tidak bereaksi karena Cu berada di sebelah kanan deret volta
2. Reaksi: Logam + Asam --> Garam + Gas Hidrogen
Mg (s) + HCl (aq) --> MgCl2 (aq) + H2 (g)
Zn (s) + H2SO4 (aq) --> ZnSO4 (aq) + H2 (g)
Ag (s) + HCl (aq) --> tidak bereaksi karena Ag berada di sebelah kanan deret volta
3. Reaksi: Logam + Asam --> Garam + Air + Gas
2Fe (s) + 6 H2SO4 (aq) --> Fe2(SO4)3 (aq) + 6 H2O (l) + 3SO2 (g)
Cu (s) + 4HNO3 (aq) --> Cu(NO3)2 (aq) + 2H2O (l) + 2NO2 (g)
Reaksi Metatesis (Pertukaran Pasangan)
Reaksi metatesis adalah reaksi pertukaran pasangan ion dari dua elektrolit.
AB + CD --> AC + BD
Pada
reaksi ini setidaknya satu produk reaksi akan membentuk endapan, gas,
atau elektrolit lemah. Gas dapat berasal dari peruraian zat hipotetis
(asam dan basa hipotetis terurai menjadi gas dan air) yang bersifat
tidak stabil seperti berikut ini:
H2CO3 --> CO2 (g) + H2O (l)
H2SO3 --> SO2 (g) + H2O (l)
NH4OH --> NH3 (g) + H2O (l)
Adapun contoh reaksi metatesis (pertukaran pasangan) adalah sebagai berikut:
1. Reaksi: Garam 1 + Asam 1 --> Garam 2 + Asam 2
AgNO3 (aq) + HBr (aq) --> AgBr (aq) + HNO3 (aq)
ZnS (s) + 2HCl (aq) --> ZnCl2 (aq) + H2S (aq)
2. Reaksi: Garam 1 + Basa 1 --> Garam 2 + Basa 2
CuSO4 (aq) + 2NaOH (aq) --> Na2SO4 (aq) + Cu(OH)2 (aq)
NH4Cl (aq) + KOH (aq) --> KCl (aq) + NH4OH (aq)
3. Reaksi: Garam 1 + Garam 2 --> Garam 3 + Garam 4
AgNO3 (aq) + NaCl (aq) --> AgCl (aq) + NaNO3 (aq)
2KNO3 (aq) + MgCl2 (aq) --> 2KCl (aq) + Mg(NO3)2 (aq)
REAKSI IDENTIFIKASI ALKOHOL PRIMER, SEKUNDER, DAN TERSIER
January 27, 2011
Alcohol
merupakan salah satu senyawa turunan alkana yang mengandung gugus
hidroksil - OH. Antara alcohol dan senyawa induknya alkana memiliki
sifat kimia dan fisika yang berbeda. Salah satunya adalah perbedaan
titik didih. Mari kita lihat perbedaan titik didih untuk jumlah atom C
yang sama.
- Titik didih metana -162oC sedangkan methanol 64,7oC
- Titik didih etana -89oC sedangkan etanol 78,3oC
- Titik didih propane -42oC sedangkan 1-propanol 97,2oC.
Apa yang menyebabkan perbedaan titik didih ini?
Ikatan
hydrogen pada molekul alcohol merupakan faktor yang menyebabkan titik
didih alcohol lebih tinggi dari pada titik didih alkana. Di sini saya
hanya akan membahas tentang reaksi identifikasi alcohol primer,
sekunder, dan tersier.
Mengenal Alkohol Primer, Sekunder, dan Tersier
Berdasarkan
jumlah atom C yang terikat pada atom C yang mengandung gugus - OH, maka
dapat dikategorikan tiga jenis alcohol, yaitu sebagai berikut:
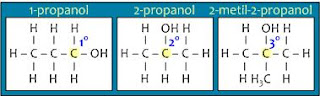
1. Alkohol primer (1o)
Alcohol primer adalah alcohol yang gugus - OH nya terikat pada atom C primer (atom C yang mengikat 1 atom C yang lain)
2. Alcohol sekunder (2o)
Alcohol sekunder adalah alcohol yang gugus - OH nya terikat pada atom C sekunder (atom C yang mengikat 2 atom C yang lain).
3. Alcohol tersier (3o)
Alcohol tersier adalah alcohol yang gugus - OH nya terikat pada atom C tersier (atom C yang mengikat 3 atom C yang lain).
Reaksi Identifikasi Alkohol Primer, Sekunder, dan Tersier
Pada alcohol primer, sekunder, dan tersier memberikan reaksi yang berbeda terhadap oksidator K2CrO7, KMnO4, dan O2.
Dengan bantuan katalis, atom O dari oksidator akan menyerang atom H
yang terikat ke atom C yang mengandung gugus - OH (atom C karbinol).
Berikut reaksi oksidasi pada masing-masing alcohol
1. Reaksi oksidasi alcohol primer
akan menghasilkan alkanal (aldehida), jika dibiarkan beberapa lama,
maka proses oksidasi akan berlanjut menghasilkan suatu asam karboksilat.
Jika kita ingin memperoleh aldehida dari proses oksidasi ini, maka
secepatnya dilakukan destilasi untuk menghindari proses oksidasi
berlanjut.














Tidak ada komentar:
Posting Komentar